Primovist 0,25 mmol/ml oldatos injekció előret.f.
Vény ellenében vagy támogatással kiadható termék
A készítmény térítési díja a felírás jogcímétől függően változhat. A foglalás kiadása a vény tulajdonosának, vagy az átvevőnek felírás igazolással kell rendelkezni!
- Gyártó/Forgalmazó:
- 00391
- Törzskönyvi szám:
- V08CA10
- Hatóanyag:
- gadoxetic acid
- Cikkszám:
- 615976
- Normatív TB támogatás:
- Nem
- Közgyógyellátásra kapható:
- Nem
A BENUVény.hu oldalunkon csak az online foglalásban résztvevő BENU gyógyszertárak kínálata látszódik. Keresse fel a gyógyszertár-keresőnket, hogy megtalálja az összes BENU Gyógyszertárat, majd vegye fel a kapcsolatot a kiválasztott patikával a megadott elérhetőségek egyikén.
Betegtájékoztató
Betegtájékoztató: Információk a felhasználó számára
Primovist 0,25 mmol/ml oldatos injekció előretöltött fecskendőben
dinátrium-gadoxetát
Mielőtt beadják Önnek ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, mert az Ön számára fontos információkat tartalmaz.
- Tartsa meg a betegtájékoztatót, mert a benne szereplő információkra a későbbiekben is szüksége lehet.
- További kérdéseivel forduljon a Primovist injekciót beadó orvoshoz.
- Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik.
Lásd 4. pont.
A betegtájékoztató tartalma:
1. Milyen típusú gyógyszer a Primovist injekció és milyen esetben alkalmazható?
2. Tudnivalók a Primovist injekció alkalmazása előtt
3. Hogyan kell alkalmazni a Primovist injekciót?
4. Lehetséges mellékhatások
5 Hogyan kell a Primovist injekciót tárolni?
6. A csomagolás tartalma és egyéb információk
1. Milyen típusú gyógyszer a Primovist injekció és milyen betegségek esetén alkalmazható?
A Primovist injekció a májon végzett mágneses rezonanciás képalkotó (MRI) eljárás kontrasztanyaga. Segítségével az esetleges májelváltozások könnyebben kimutathatók és diagnosztizálhatók. A máj rendellenességei – azok száma, mérete, és eloszlása – jobban értékelhetők. A Primovist injekció segíthet az orvosnak a rendellenességek természetének meghatározásában is, ezáltal megnöveli a diagnózis megbízhatóságát.
A Primovist injekció egy intravénás alkalmazásra szánt oldat.
Ez a gyógyszer kizárólag diagnosztikai célra alkalmazható.
Az MRI egy orvosi diagnosztikai képalkotó rendszer, amely a normál és beteg szövetben előforduló vízmolekulák észlelését követően alkot képeket. Ezt mágnesek és rádióhullámok összetett rendszerével valósítja meg.
2. Tudnivalók a Primovist injekció alkalmazása előtt
Ne alkalmazza a Primovist injekciót:
- ha allergiás a dinátrium-gadoxetátra vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére.
Figyelmeztetések és óvintézkedések
Beszéljen kezelőorvosával a Primovist alkalmazása előtt, ha
- asztmás vagy allergiás (pl. szénanátha, csalánkiütés), vagy az volt korábban
- korábban egy kontrasztanyag beadása bármiféle reakciót váltott ki Önnél
- veséje nem működik megfelelően. Egyes gadolínium-tartalmú kontrasztanyagok alkalmazásával összefüggésben, vesebetegségben szenvedő betegek esetében, úgynevezett nefrogén szisztémás fibrózis (NSF) előfordulásáról számoltak be. Az NSF a bőr és a kötőszövetek elvékonyodásával járó megbetegedés. Az NSF legyengüléssel járó ízületi mozgásképtelenséget, izomgyengeséget vagy a belső szervek működésének károsodását eredményezheti, ami esetlegesen életveszélyes is lehet.
- súlyos szív- vagy érrendszeri betegségben szenved
- alacsony a kálium vérszintje
- Önnek vagy valamely családtagjának egy úgynevezett hosszú-QT-szindróma nevű szívritmuszavara van, vagy volt
- bármely korábban alkalmazott gyógyszer hatására megváltozott a szívritmusa
- a szervezetében szívritmus-szabályozó készülék (pacemaker) vagy bármilyen beültetett fémimplantátum, vagy egyéb sín/kapocs található.
A Primovist injekció alkalmazását követően órákkal vagy napokkal később is jelentkezhetnek allergiaszerű reakciók, késői reakció formájában (lásd. 4. pont).
Feltétlenül tájékoztassa kezelőorvosát:
ha a veséje nem működik megfelelően
ha Ön nemrégiben májátültetésben részesült, vagy a közeljövőben arra vár.
Mielőtt a Primovist injekció alkalmazása mellett döntene, orvosa vérvizsgálatot írhat elő, hogy ellenőrizze az Ön veseműködését, különösen akkor, ha Ön 65 éves vagy idősebb.
A gadolínium felhalmozódása a szervezetben
A Primovist egy gadolínium nevű fémet tartalmaz. Ez az alkotórész teszi lehetővé a vizsgálat elvégzését. Vizsgálatok igazolták, hogy a gadolínium kis mennyiségben visszamaradhat a szervezetben, többek között az agyban. Nem tapasztaltak mellékhatást azzal kapcsolatban, hogy a gadolínium visszamarad az agyban.
Gyermekek és serdülők
A Primovist injekció hatékonysága és biztonságossága 18 év alatti betegeknél nem kellően megalapozott, mivel még nem áll rendelkezésre elegendő klinikai tapasztalat. A Primovist injekció gyermekeknél történő alkalmazásával kapcsolatban a betegtájékozható végén találhat további információt.
Egyéb gyógyszerek és a Primovist
Feltétlenül tájékoztassa kezelőorvosát a jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről. Különösen igaz ez az alábbi gyógyszerekre:
- béta-blokkoló szerek, magas vérnyomás vagy egyéb szívbetegségek kezelésére szolgáló gyógyszerek
- szívritmust vagy pulzusszámot befolyásoló gyógyszerek, mint pl. amiodaron, szotalol
rifampicin: tbc (tüdőgümőkór), illetve bizonyos más fertőzések kezelésére szolgáló gyógyszer.
Terhesség és szoptatás
Terhesség
A gadoxetát átjuthat a méhlepényen. Nem ismert, hogy ez hatással van-e a magzatra. Feltétlenül tájékoztassa kezelőorvosát, ha Ön terhes, vagy úgy gondolja, hogy teherbe eshet, mivel a Primovist injekció alkalmazása kerülendő terhességben, kivéve, ha az alkalmazás mindenképpen szükséges.
Szoptatás
Tájékoztassa kezelőorvosát, ha Ön szoptat, vagy szoptatás előtt áll. Kezelőorvosa megbeszéli Önnel, hogy folytassa-e a szoptatást, vagy függessze fel azt 24 órára a Primovist injekció beadása után.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
A Primovist nem befolyásolja a gépjárművezetéshez és a gépek kezeléséhez szükséges képességeket.
A Primovist injekció nátriumot tartalmaz
Ez a gyógyszer 82 mg nátriumot (a konyhasó fő összetevője) tartalmaz adagonként (egy 70 kg‑os, átlagos testsúlyú emberre számolva), ami megfelel a nátrium ajánlott maximális napi bevitel 4,1%‑ának felnőtteknél.
3. Hogyan kell alkalmazni a Primovist injekciót?
A Primovist injekciót egy vékony tű segítségével adják be a vénájába. A Primovist injekciót közvetlenül az MRI-vizsgálat előtt adják be.
Az injekció után legalább 30 percig megfigyelik Önt.
A készítmény ajánlott adagja
0,1 ml Primovist testtömeg-kilogrammonként.
Adagolás különleges betegcsoportokban
A Primovist injekció alkalmazása nem ajánlott súlyos vesebetegségben, valamint olyan betegeknél, akik nemrégiben májátültetésen estek át, vagy akikre ilyen műtét vár a közeljövőben. Ha azonban a Primovist injekció alkalmazása elkerülhetetlen, Ön a felvétel készítése során csak egy adagot kaphat, és legkorábban 7 nap múlva kerülhet sor ilyen kontrasztanyag ismételt alkalmazására.
Idősek
Nincs szükség a dózis módosítására, ha Ön 65 éves vagy idősebb, de szükséges lehet, hogy vérvizsgálatot végezzenek önnél a veseműködés ellenőrzésére.
Ha az előírtnál több Primovist injekciót kapott:
A túladagolás valószínűtlen. Ha ez mégis előfordul, akkor az orvos kezelni fogja a megjelenő tüneteket.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
A legtöbb mellékhatás enyhe vagy mérsékelt.
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát.
Egyéb kontrasztanyagokhoz hasonlóan, ritka esetben allergiaszerű reakciók jelentkezhetnek. Késői reakciók órákkal vagy napokkal a Primovist beadása után is előfordulhatnak.
A legsúlyosabb mellékhatás, amely a Primovist injekciót kapó betegeknél előfordulhat, az anafilaktoid sokk (egy súlyos allergiaszerű reakció).
Azonnal közölje kezelőorvosával, ha a következő tünetek bármelyikét észleli, vagy légzési nehézségei vannak:
- alacsony vérnyomás
- a nyelv, a torok vagy az arc duzzanata
- orrfolyás, tüsszögés, köhögés
- vörös, könnyező és viszkető szemek
- gyomorfájás/hasfájás
- csalánkiütés
- a bőrérzékelés, illetve a bőr érzékenységének csökkenése; viszkető, sápadt bőr.
További lehetséges mellékhatások:
Gyakori (10 betegből legfeljebb 1 beteget érinthet)
- fejfájás
- hányinger
Nem gyakori (100 betegből legfeljebb 1 beteget érinthet)
- szédülés
- zsibbadás és bizsergés
- ízérzékelési, illetve szaglási zavar
- kipirulás
- magas vérnyomás
- légzési nehézségek
- hányás
- szájszárazság
- bőrkiütés
- súlyos viszketés, amely érintheti az egész testet, illetve a szemet
- hátfájdalom, mellkasi fájdalom
- injekció beadásának helyén fellépő reakciók, pl.: égő érzés, hidegérzet, irritáció, fájdalom
- forróságérzet
- hidegrázás
- fáradtság
- normálistól eltérő közérzet
Ritka (1000 betegből legfeljebb 1 beteget érinthet)
- képtelenség a nyugodt egy helyben ülésre vagy állásra
- kontrollálhatatlan remegés
- gyors szívverés érzése
- szabálytalan szívverés (szívblokk tünete)
- kellemetlen érzés a szájban
- fokozott nyálelválasztás
- bőrkiütések vörös göbökkel vagy foltokkal
- fokozott verejtékezés
- kellemetlen érzés, rossz általános közérzet
Nem ismert (a gyakoriság a rendelkezésre álló adatokból nem állapítható meg)
- gyors szívverés
- nyugtalanság
A laboratóriumi értékek megváltozhatnak, röviddel a Primovist injekció alkalmazása után. Ezért vér- és/vagy vizeletvizsgálat esetén tájékoztassa az egészségügyi személyzetet arról, ha a közelmúltban Primovist injekciót kapott.
Más gadolínium-tartalmú kontrasztanyagok alkalmazásával összefüggésben a bőr megkeményedését okozó, esetleg a lágy szöveteket és a belső szerveket is érintő elváltozásról, úgynevezett nefrogén szisztémás fibrózisról (NSF-ről) számoltak be.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti az V. függelékben található elérhetőségeken keresztül.
A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell a Primovist injekciót tárolni?
A gyógyszer gyermekektől elzárva tartandó!
A dobozon és a tartályon feltüntetett lejárati idő után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Ez a gyógyszer nem igényel különleges tárolást.
A készítményt a felbontás után azonnal fel kell használni.
Használat előtt vizuálisan meg kell vizsgálni.
Jelentős elszíneződés, szemcsés anyag jelenléte vagy sérült tartály esetén a kontrasztanyag nem használható.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel . Ezek az intézkedések elősegítik a környezet védelmét.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz a Primovist injekció?
- A készítmény hatóanyaga: a dinátrium-gadoxetát (Gd-EOB-DTPA-dinátrium). 0,25 mmol dinátrium-gadoxetátot tartalmaz milliliterenként, amely megfelel 181,43 mg dinátrium-gadoxetátnak.
- Egyéb összetevők: trinátrium-kaloxetát, trometamol, sósav és nátrium-hidroxid (mindkettő pH‑beállítás céljából), injekcióhoz való víz.
Egy 5 ml oldatot tartalmazó fecskendő 907 mg dinátrium-gadoxetátot tartalmaz.
Egy 7,5 ml oldatot tartalmazó fecskendő 1361 mg dinátrium-gadoxetátot tartalmaz. [csak üvegfecskendő].
Egy 10 ml oldatot tartalmazó fecskendő 1814 mg dinátrium-gadoxetátot tartalmaz.
Milyen a Primovist injekció külleme és mit tartalmaz a csomagolás?
A Primovist tiszta, színtelen vagy halványsárga színű, látható részecskéktől mentes oldat.
1 db, 5 db vagy 10 db előretöltött fecskendő, melynek tartalma fecskendőnként:
5 ml oldatos injekció (10 ml-es előretöltött üveg-/műanyag fecskendőben)
7,5 ml oldatos injekció (10 ml-es előretöltött üvegfecskendőben) [csak üvegfecskendő]
10 ml oldatos injekció (10 ml-es előretöltött üveg-/műanyag fecskendőben)
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
A forgalomba hozatali engedély jogosultja és a gyártó
A forgalomba hozatali engedély jogosultja
Bayer AG
51368 Leverkusen
Kaiser-Wilhelm-Allee
Németország
Gyártó
Bayer AG
13353 Berlin, Müllerstr. 178.
Németország
OGYI-T-9837/01
Primovist 0,25 mmol/ml oldatos injekció (előretöltött üvegfecskendőben) 1×10 ml
OGYI-T-9837/02
Primovist 0,25 mmol/ml oldatos injekció (előretöltött üvegfecskendőben) 5×10 ml
OGYI-T-9837/03
Primovist 0,25 mmol/ml oldatos injekció (előretöltött üvegfecskendőben) 10×10 ml
OGYI-T-9837/04
Primovist 0,25 mmol/ml oldatos injekció (előretöltött üvegfecskendőben) 1×7,5 ml
OGYI-T-9837/05
Primovist 0,25 mmol/ml oldatos injekció (előretöltött üvegfecskendőben) 5×7,5 ml
OGYI-T-9837/06
Primovist 0,25 mmol/ml oldatos injekció (előretöltött üvegfecskendőben) 10×7,5 ml
OGYI-T-9837/13
Primovist 0,25 mmol/ml oldatos injekció (előretöltött műanyag fecskendőben) 1×5 ml
OGYI-T-9837/14
Primovist 0,25 mmol/ml oldatos injekció (előretöltött műanyag fecskendőben) 5×5 ml
OGYI-T-9837/15
Primovist 0,25 mmol/ml oldatos injekció (előretöltött műanyag fecskendőben) 10×5 ml
OGYI-T-9837/16
Primovist 0,25 mmol/ml oldatos injekció (előretöltött műanyag fecskendőben) 1×10 ml
OGYI-T-9837/17
Primovist 0,25 mmol/ml oldatos injekció (előretöltött műanyag fecskendőben) 5×10 ml
OGYI-T-9837/18
Primovist 0,25 mmol/ml oldatos injekció (előretöltött műanyag fecskendőben) 10×10 ml
A betegtájékoztató legutóbbi felülvizsgálatának dátuma: 2024. december.
-----------------------------------------------------------------------------------------------------------------------
Az alábbi információk kizárólag egészségügyi szakembereknek szólnak:
- Vesekárosodás
A Primovist injekció alkalmazása előtt valamennyi betegnél ajánlott laboratóriumi vizsgálatot végezni a beszűkült vesefunkció kiszűrésére.
Egyes gadolínium-tartalmú kontrasztanyagok alkalmazásával összefüggésben nefrogén szisztémás fibrózisról (NSF-ről) számoltak be, súlyos, akut vagy krónikus veseelégtelenségben szenvedő betegek esetében (GFR < 30 ml/perc/1,73 m2). A májtranszplantált betegek különösen veszélyeztetettek, mivel a Primovist injekció alkalmazása esetén az akut veseelégtelenség előfordulási aránya magas ebben a betegcsoportban. Mivel a Primovist injekció alkalmazása esetén fennáll az NSF lehetősége, a készítmény használatát kerülni kell
- súlyos vesekárosodásban szenvedő betegeknél,
- májtranszplantáció perioperatív szakaszában,
kivéve, ha a diagnosztikus információ alapvető fontosságú, és az nem szerezhető be natív (nem kontrasztanyagos) MRI-vizsgálattal. Ha a Primovist injekció alkalmazása elkerülhetetlen, a dózis nem haladhatja meg a 0,025 mmol/ttkg-ot. A felvétel készítése során nem adható egynél több adag. Az ismételt alkalmazásra vonatkozó adatok hiányában a Primovist injekció nem ismételhető, kivéve, ha a két beadás között legalább 7 nap eltelt.
Mivel a gadoxetát veseclearance-e időseknél csökkent lehet, 65 éves vagy idősebb betegek esetében különösen fontos a beszűkült vesefunkció kiszűrése.
A Primovist injekció alkalmazását követően rövid idővel végzett hemodialízis hasznos lehet a Primovist injekció szervezetből való eltávolítása szempontjából. Nincs olyan bizonyíték azonban, mely indokolná a hemodialízis bevezetését az NSF megelőzése vagy kezelése érdekében olyan betegeknél, akik még nem állnak hemodialízis-kezelés alatt.
- Terhesség és szoptatás
A Primovist injekció alkalmazását kerülni kell a terhesség alatt, kivéve, ha a nő klinikai állapota szükségessé teszi a gadoxetát alkalmazását.
A szoptatás folytatásáról, vagy a Primovist injekció beadása utáni 24 órára történő felfüggesztéséről az orvosnak és a szoptató anyának kell dönteni.
- Gyermekek és serdülők
Megfigyeléses vizsgálatot végeztek 52 gyermek (2 hónaposnál idősebb és 18 évesnél fiatalabb) részvételével. A betegek feltételezett, vagy ismert gócos májelváltozásait Primovist-kontrasztanyaggal erősített MRI-vizsgálat segítségével értékelték ki. További diagnosztikus információ származott a máj kontrasztanyag nélküli és kontrasztanyaggal erősített MR-vizsgálati eredményeinek a kontraszterősítés nélküli MR-eredményekkel történő összehasonlításából. Jelentettek súlyos nemkívánatos eseményeket, azonban a klinikai vizsgáló egyik esetben sem talált összefüggést a Primovist injekció használatával. Ezen vizsgálat retrospektív természete és kis betegszáma miatt erre a betegcsoportra vonatkozóan, a hatásossággal és biztonságossággal kapcsolatban nem vonhatóak le végleges következtetések.
- Beadás előtt
A Primovist injekció tiszta, színtelen vagy halványsárga színű, látható részecskéktől mentes oldat. Használat előtt vizuálisan kell megvizsgálni. Jelentős elszíneződés, szemcsés anyag jelenléte vagy sérült tartály esetén a kontrasztanyag nem használható.
- Alkalmazás
Az Primovist-oldatot hígítatlanul, intravénás bolus injekció formájában kell beadni, kb. 2 ml/másodperc sebességgel. Ezután az intravénás kanült és szereléket steril fiziológiás (9 mg/ml-es [0,9%-os]) konyhasóoldattal át kell öblíteni.
- Az injekció beadása után a beteget legalább 30 percen keresztül meg kell figyelni
- A Primovist injekciót egyéb készítményekkel tilos elegyíteni.
- Az intramuscularis alkalmazást szigorúan el kell kerülni.
- Kezelés
A Primovist injekció használatra kész oldat.
Az előretöltött fecskendőt közvetlenül a vizsgálat előtt kell előkészíteni.
A zárókupakot közvetlenül a felhasználás előtt kell eltávolítani a fecskendőről.
Az egy vizsgálat során fel nem használt kontrasztanyagot a helyi előírásoknak megfelelően kell megsemmisíteni.
Annak érdekében, hogy a felhasznált gadolínium-tartalmú kontrasztanyag pontosan beazonosítható legyen, az injekciós üvegeken/fecskendőkön lévő, lehúzható betegkövető címkét be kell ragasztani a beteg dokumentációjába. A felhasznált adagot szintén dokumentálni kell.
Amennyiben elektronikus kórlapot használnak, a termék nevét, gyártási számát és a dózist be kell vezetni a beteg elektronikus kórlapjába.
[Csak üvegfecskendő esetén]
|
| |
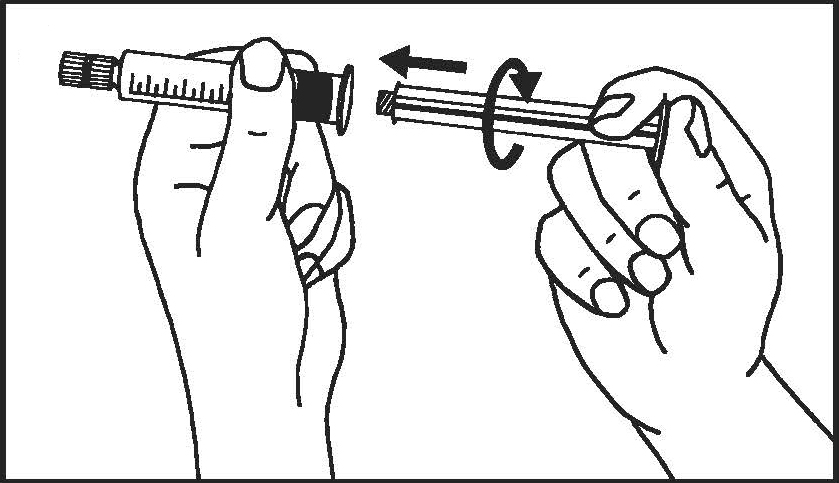
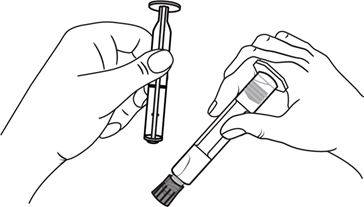
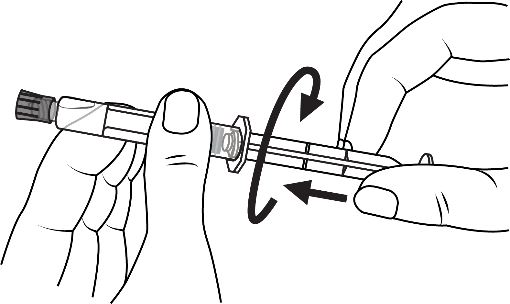
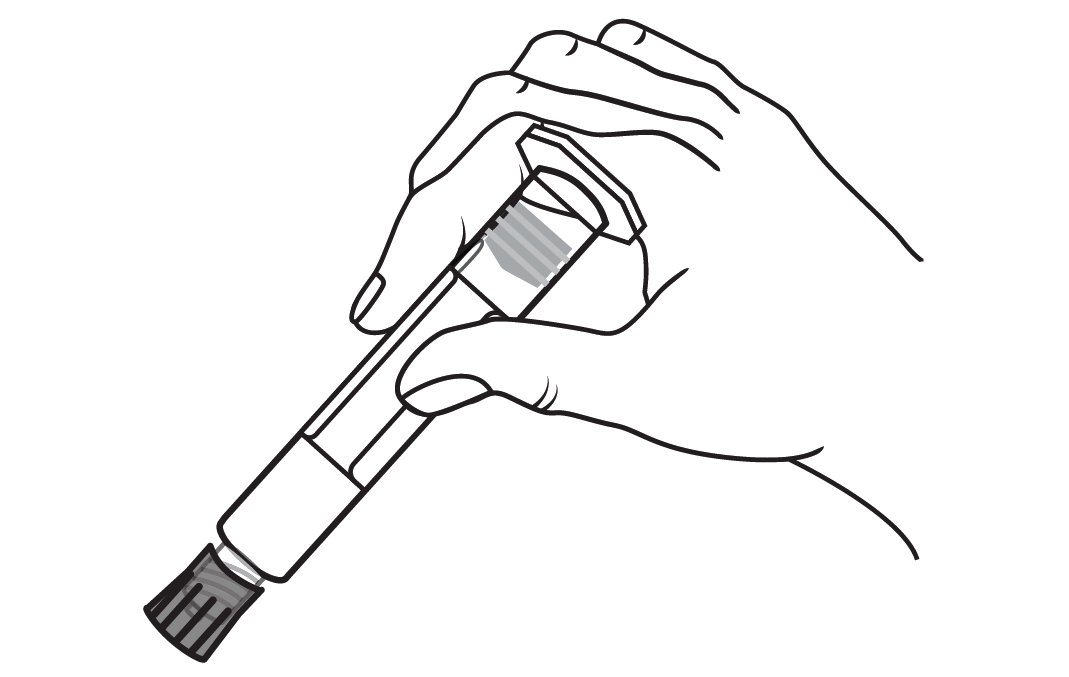
1. Nyissa ki a csomagolást! | 2. Csavarja fel a dugattyút a fecskendőre! | |
|
| |
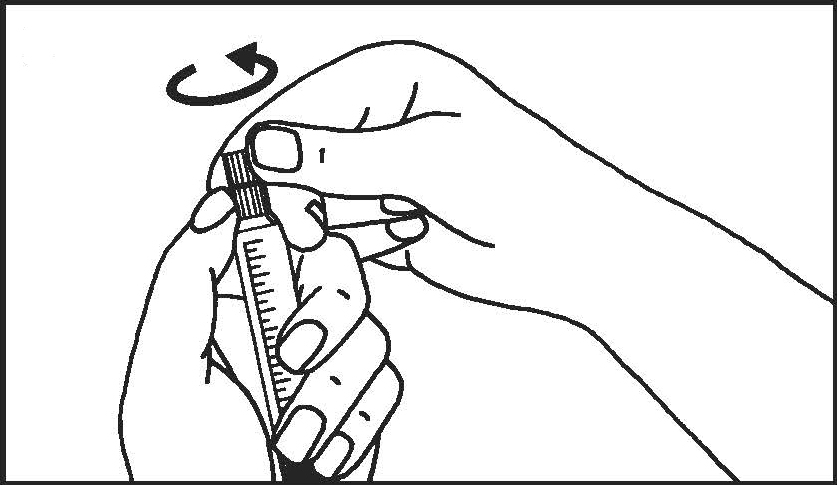
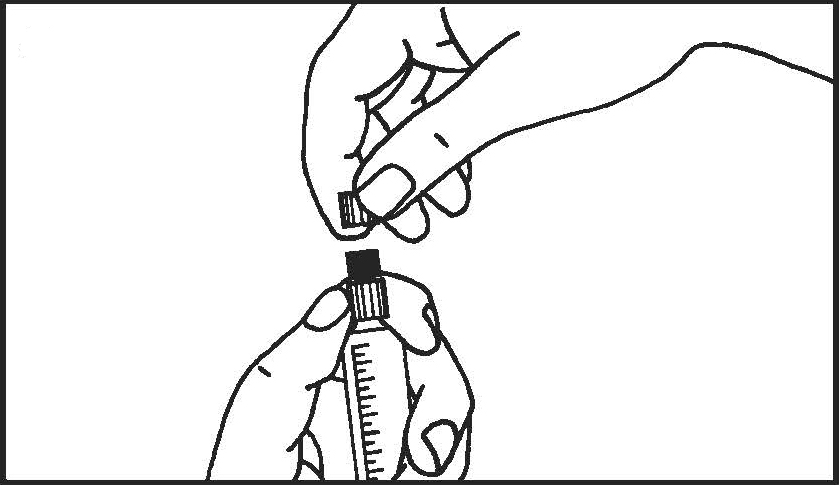
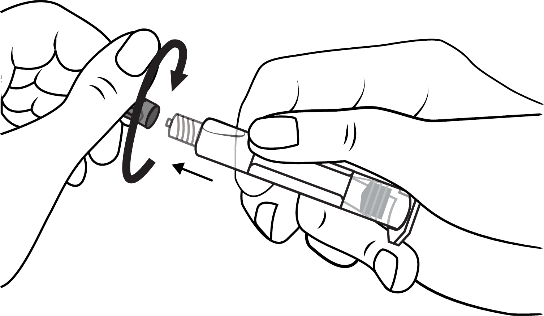
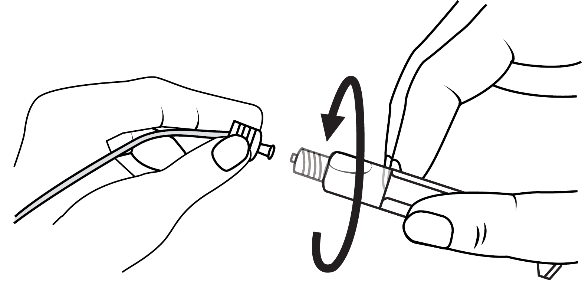
3. Csavarja el a védőkupakot! | 4. Távolítsa el a védőkupakot! | |
|
| |
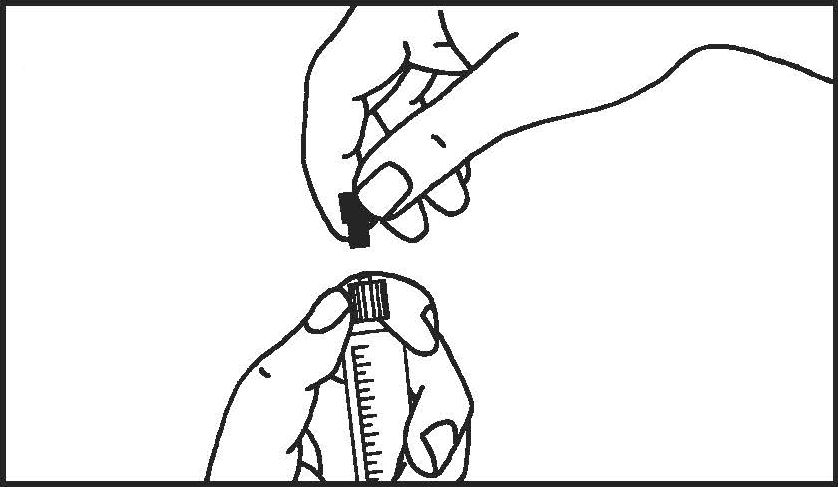
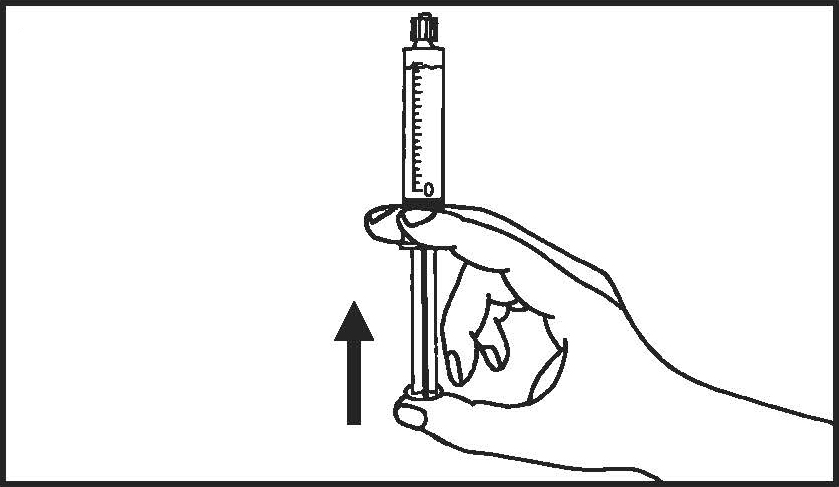
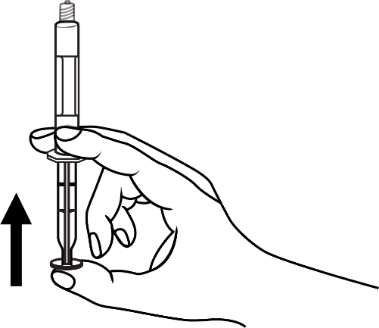
5. Távolítsa el a gumidugót! | 6. Távolítsa el a légbuborékokat a fecskendőből! |
[Csak műanyag fecskendő esetén]
Kézi beadás
| Beadás injektorral
|